
Простые технические эксперименты очень полезно делать с детьми, это и совместное времяпровождение, и прививание навыков, и понимание маленькими конструкторами, основ, того, что батоны, как в известном мультике, не на деревьях растут.
В этот раз, мы решили сделать простейший химический источник тока, и попытаться его применить для чего ни будь практического. Говоря о практическом применении, стоит вспомнить, что всего несколько поколений назад, радиолюбителям, для питания их батарейных радиоприемников и усилителей, предлагались к самостоятельному изготовлению несколько типов гальванических элементов или аккумуляторов. Это элементы Лекланше и Попова [1] стр. 9…18, или свинцово-поташный или газовый аккумулятор [1], стр. 22…28. Несколько, относительно сильноточных элементов соединяли в батарею накаливания (нити накаливания радиоламп), десятки элементов поменьше, в анодную батарею, напряжение которой, могло достигать 60-80 вольт. Батареи были «мокрыми» - с жидким электролитом и требовали ухода и обслуживания.
Итак, гальванический элемент, несколько слов «как?» и «почему?». Электрический ток возникает при взаимодействии разных металлов. При этом возникает различная разность потенциалов (напряжение). Еще в 1793 году Алессандро Вольта, конструируя гальванический элемент (Вольтов столб), установил относительную активность известных тогда металлов: Zn, Pb, Sn, Fe, Cu, Ag, Au. «Сила» гальванического элемента оказывалась тем больше, чем дальше стояли друг от друга металлы в этом ряду (ряд напряжений).

«Аутентичный» Вольтов столб, возможно – тот самый.
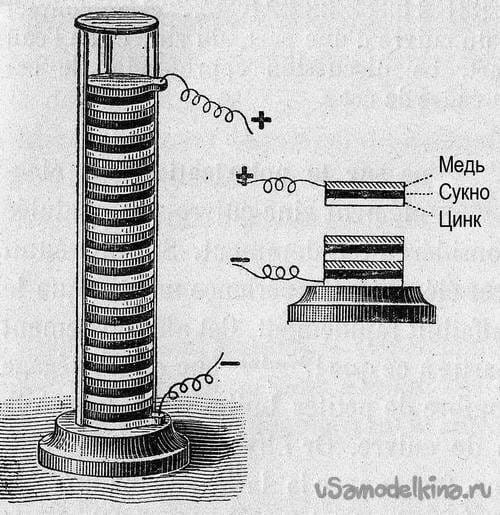
Устройство Вольтова столба.
Позже, для упорядочивания данных, приняли за ноль отсчета потенциал «водородного электрода». Измерив потенциал металлов в паре с ним, расположили подопытные металлы в ряд. Полученная таблица получила название «Электрохимический ряд напряжений металлов» и в кабинете химии, обязана висеть рядом с периодической системой и портретом Дмитрия Ивановича.


Ряд напряжений металлов – полезнейшая штуковина, в нашем случае, мы, как и Алессандро Вольта, будем знать – чем дальше металлы отстоят друг от друга, тем большее напряжение удастся получить.
В своих опытах, как и классики, мы использовали медь и цинк. При погружении пластинок в электролит, между ним и цинковой пластинкой, происходит химическая реакция, в результате которой на пластинке скапливаются отрицательные заряды и она заряжается отрицательно. В результате реакции происходящей в гальваническом элементе, цинковый электрод постепенно растворяется.
На медном электроде, при работе гальванического элемента, образуются мельчайшие пузырьки водорода, изолирующие поверхность меди от электролита. Явление называется газовой поляризацией, в гальваническом элементе оно вредно, с ним борются. Для удаления выделяющегося водорода, в электролит вводятся вещества связывающие водород, называемые деполяризаторами. В их роли часто выступают соединения марганца, медный купорос. В простых опытах, можно применить аптечный перманганат калия.
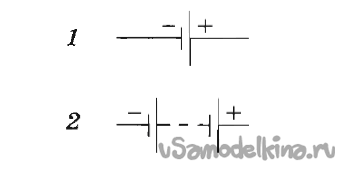
На принципиальных электрических схемах, гальванический элемент или аккумулятор обозначается так - 1, а батарея (несколько соединенных) элементов или аккумуляторов - 2.
Что мы использовали для эксперимента.
Приборы и материалы.
Для сборки гальванических элементов, в качестве медных электродов, можно использовать проволоку, провод, фольгу. Цинк можно извлечь из сухих элементов, применить оцинкованные изделия. Вместо цинкового, можно попробовать применить электрод из алюминия или железа. Поваренная соль для электролита, немного мягкого монтажного провода. Непременно нужен вольтметр или мультиметр, кусачки, ножницы. В качестве сосудов, можно применять неметаллические емкости подходящего размера. Стеклянные, удобнее легких пластиковых стаканчиков – они тяжелее, устойчивее, опрокинуть их труднее. Очень хорошо, если найдется слаботочная низковольтная нагрузка – простое радио, кварцевые часы, и т.п.
«Высоковольтная» батарея из проволоки и саморезов.
Прельстившись простотой деталей, и относительно высоким получаемым напряжением, мы попытались собрать такую батарею. Здесь применяется «классическая» пара металлов – медь-цинк. Идея состоит в применении в качестве цинкового электрода, оцинкованного крепежа. Изящно. Понятно, что на длительную работу, такой элемент не рассчитан – тонкий слой цинка быстро растворится, однако, для кратковременного эксперимента это и не важно. Зато оцинкованных шурупов или винтиков везде полно.
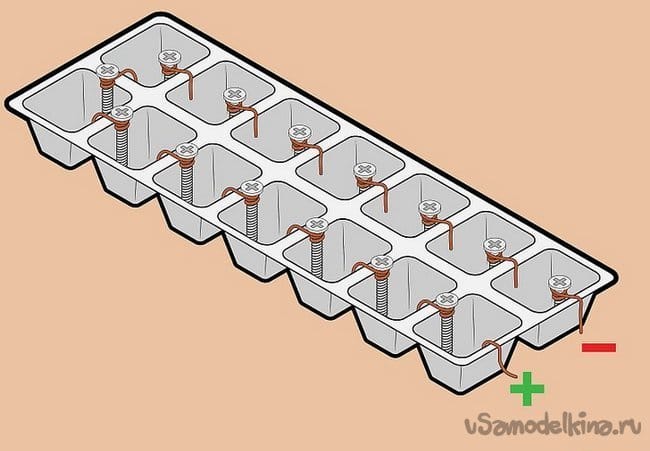
В качестве медного электрода применена проволока – также, широко доступный материал, кроме того – удобнейший монтаж элементов в батарею – все элементы соединены последовательно – плюс одного к минусу следующего. При этом напряжение суммируется, ток остается прежним.
Приступим.
После подбора необходимого количества оцинкованного крепежа нужной длины, мы нашли подходящую медную проволочку. Это обмоточный провод в лаковой изоляции. Диаметр провода около 0,5 мм.

Полюшка зачищает лаковую изоляцию, несколько раз, с усилием протягивая провод, через сложенную вдвое шлифовальную шкурку средней крупности.


Затем, подготавливает пары электродиков – под шляпкой самореза, плотно наматывает два-три витка проволоки и обрезает лишнее.

Сборка батареи – в качестве емкости использовано корытце для замораживания льда. Можно применить и ячейки от коробочных конфет, правда, они понежнее. После установки электродов на стенках между ячейками, заполняем емкости электролитом. Мы использовали раствор поваренной соли – столовую ложку с горкой на 0,5 л теплой воды. Для заполнения очень удобно применять медицинскую спринцовку.

— Очень хочется произвести на вас приятное впечатление.
— Вам это удалось… уже.
— Усилить хочется.
«Служебный роман».

Мы нашли еще несколько шурупов для электродов и добавили элементов в батарее, вот, что у нас получилось. Напряжение на высокоомной нагрузке (входное сопротивление цифрового вольтметра) изрядное, но на любой, сколь ни будь заметной нагрузке, сильно падает.
Попытаемся сделать аналогичный гальванический элемент (батарею) с электродами побольше.
В качестве емкости, мы применили поллитровую баночку (две), в нее поместятся пластинки значительной площади. В качестве электродов мы взяли тонкую медную фольгу и цинк – остатки стаканчика от фабричного «сухого» элемента, разобранного при добыче графита для огнеупорной обмазки.

Остатки засохших кристаллических солей мы счистили проволочной щеткой и вырезали большими ножницами две пластинки, примерно равной площади. Из медной фольги, вырезали две соответствующих полосочки. Тоже ножницами. Получили две пары электродов, которыми снарядили наши элементы, не мудрствуя, загнув их края на горлышке банки.


В емкости побольше, приготовили электролит – поваренную соль, растворили в теплой воде, концентрация та же, и залили подготовленные элементы.


Два элемента мы соединили последовательно, при помощи кусочка монтажного провода и двух зажимов «крокодил». Та-ак, прекрасно, напряжение батареи близко к стандартному «пальчиковому», попробуем использовать. Один элемент напряжением 1.5 В используется в электромеханических часах, кроме того, ток потребления часов очень мал и наша батарея вполне сможет его осилить.

Из часов мы извлекли штатный элемент питания и к клеммам присоединили по кусочку монтажного провода. Соблюдая полярность (медная пластинка – «+», цинковая – «-»), подключили наши часы к самодельной батарее, вуаля! Часы работают, напряжение «проседает» до 1,3 В. Часы, преотлично работали несколько часов, пока мы всем не похвастались (однако колдун!) потом надоело.

На дорожку.
Внутреняя конституция у любого ребенка такова, что внимание на одном предмете, он способен сосредотачивать не более 15…20 минут, и все занятия с детьми следует планировать так, чтобы они укладывались в это время, либо переключаться между разными занятиями, иначе оба намучаетесь.
В качестве нагрузки, лучше применить, что ни будь движущееся или светящееся – цифры на вольтметре впечатляют ум, но не сердце. Кроме часов и калькуляторов, наверняка вызовет восхищение, работа от самодельной батареи небольшого радиоприемника (как вариант - самодельного!).
При долговременном использовании, электролит элементов стоит предохранить от пыли и испарения, и позаботиться о деполяризаторе - ну, хотя бы закупорив баночку обрезком полиэтиленовой пленки с резинкой и добавив в электролит перманганат калия. Более того, лучше сразу собирать помянутый элемент Попова.
Кроме оцинкованных саморезов, можно применить оцинкованную листовую сталь, для крупных элементов это удобнее - на время эксперимента можно получить значительный ток и запитать что ни будь (пошевелив пальцами в воздухе) этакое.
Список используемой литературы.
1. П.Стрелков. Знай и умей. Пионер-электротехник. Детгиз. 1960 г.
2. В.С.Полосин, В.Г.Прокопенко. Практикум по методике преподавания химии. Москва, «Просвещение», 1989 г. Стр.202,203.
Становитесь автором сайта, публикуйте собственные статьи, описания самоделок с оплатой за текст. Подробнее здесь.




